Actualidad
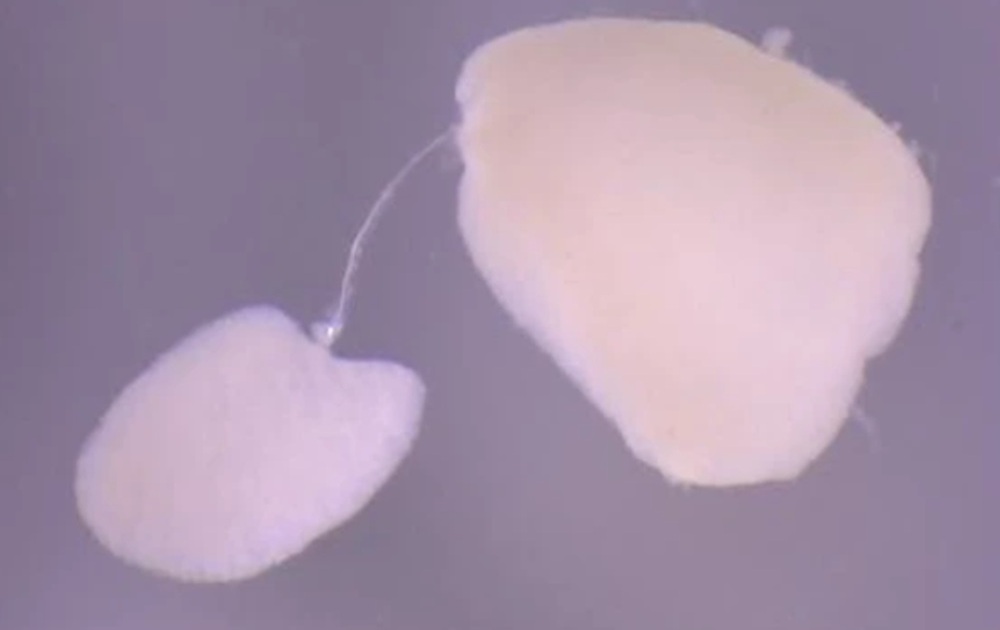
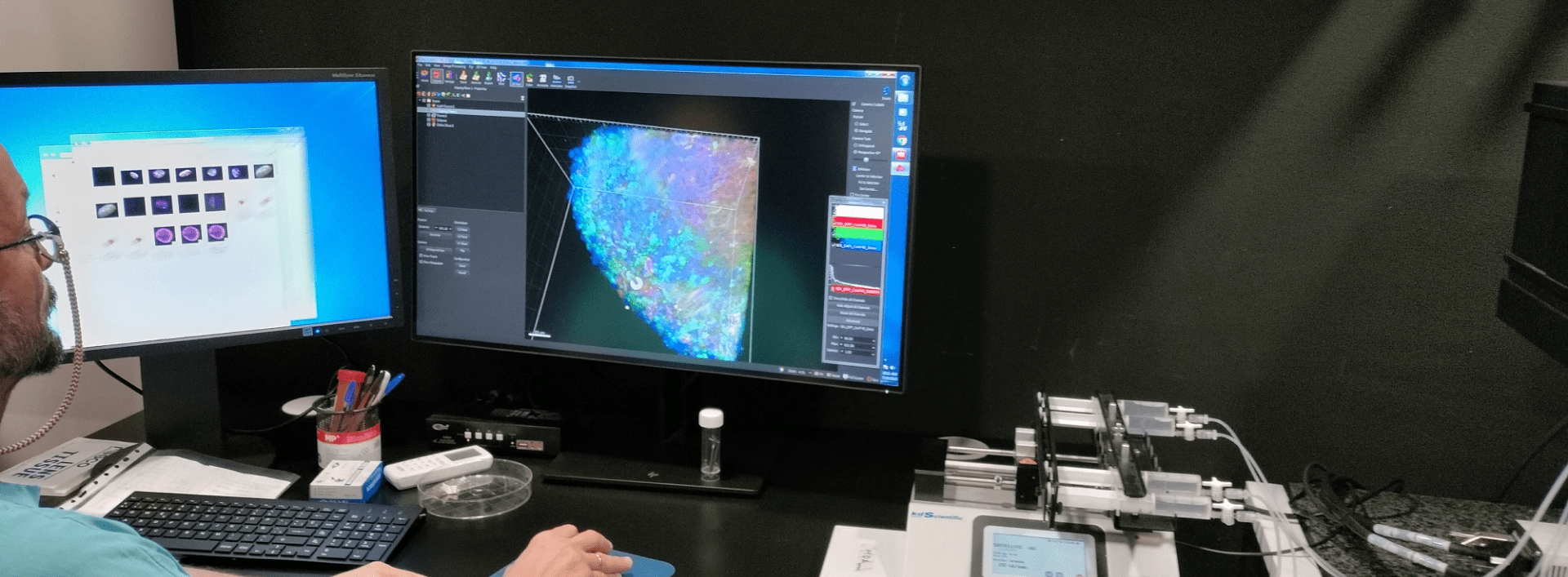
Organoides derivados de pacientes de glioma para personalizar el estudio y futuro tratamiento de estos tumores cerebrales
Una investigación liderada desde el Instituto de Salud Carlos III (ISCIII), la Universidad Francisco de Vitoria (UFV) y el Grupo Hospitalario Vithas, aporta novedades clave en el desarrollo de organoides de glioma para la investigación y el abordaje clínico de este tipo de tumores, los más comunes en adultos entre los tipos de cáncer cerebral. Los resultados del estudio se han publicado en la revista Biomarker Research. Los organoides son 'mini-órganos' desarrollados en laboratorio a partir de células humanas, que imitan la actividad de los órganos humanos, lo que facilita la investigación de enfermedades y la búsqueda de posibles tratamientos. En esta investigación, el equipo del ISCIII ha generado organoides tumorales derivados de pacientes afectados de glioma, y ha logrado que ‘imiten’ con fiabilidad la heterogeneidad celular tumoral, la arquitectura histológica y las firmas moleculares de los tumores ‘madre’, preservando características clínicamente relevantes, perfiles inmunitarios, estructuras vasculares y las características de cada subtipo tumoral. De esta manera, el estudio establece “una plataforma fiel y clínicamente relevante que puede acelerar la investigación, el cribado y reposicionamiento de fármacos ya aprobados hacia pacientes con glioma”, según explica Ángel Ayuso, autor principal del trabajo e investigador en la Unidad Funcional de Investigación en Enfermedades Crónicas (UFIEC) del Instituto. También firman la publicación Pilar Sánchez Gómez y María Castelló Pons, de la citada Unidad. Más concretamente, los organoides de glioma generados en esta investigación mantienen a largo plazo una mutación clave, denominada IDH1 R132H, algo que otros cultivos 2D suelen perder, por lo que permiten modelar una biología tumoral muy difícil de reproducir en el laboratorio. Los organoides también conservan el fenotipo inmunitario ‘frío’ del glioblastoma, con predominio mieloide y casi ausencia de linfocitos T, aportando datos que ayudan a explicar el limitado éxito de diversas inmunoterapias actuales. Además, gracias a análisis por microscopía electrónica de transmisión (TEM) en este tipo de organoides, se ha confirmado que cuentan con una complejidad ultraestructural superior a la aportada por estudios con otras líneas celulares, incluyendo interacciones neurona-glía y preservación de orgánulos: “Lo más innovador es un ‘pipeline’ que integra cribado ‘in silico’ con un modelo ‘in vitro’ de alta fidelidad: cruzamos perfiles de expresión de los organoides con bases de datos de sensibilidad a fármacos para priorizar terapias potencialmente personalizadas en un plazo compatible con la práctica clínica”, según señalan el investigador del ISCIII y Noemí García Romero, profesora del Grado en Biomedicina de la UFV y co-investigadora principal del trabajo. Álvaro Monago Sánchez, investigador predoctoral de la UFV, añade que los datos obtenidos en la investigación “respaldan la inclusión de dos nuevos compuestos, alectinib y ruxolitinib, en futuras investigaciones clínicas para el tratamiento del glioma". De izquierda a derecha, parte del equipo responsable del estudio: Angel Ayuso, Investigador Senior en la UFIEC-ISCIII; Noemi García, co-investigadora principal, de la UFV; Alvaro Monago, investigador predoctoral, y Laura Mateos, también investigadora predoctoral. En definitiva, los resultados del estudio permiten avanzar hacia modelos de organoides específicos e individualizados para cada paciente, y presenta una plataforma fácil de utilizar en la búsqueda de tratamientos más eficaces y personalizados. • Referencia del artículo: Monago-Sánchez, A., Mateos-Madrigal, L., Carrión-Navarro, J. et al. Precision oncology in a dish: patient-derived glioma organoids to guide novel therapeutic strategies. Biomark Res 14, 27 (2026). https://doi.org/10.1186/s40364-026-00894-3 Noticias relacionadas: - Organoides cerebrales humanos: Modelos complejos y prometedores para estudiar el cerebro - Organoides que 'imitan' el cerebro humano para facilitar el desarrollo de terapias para enfermedades neurológicas
Saber más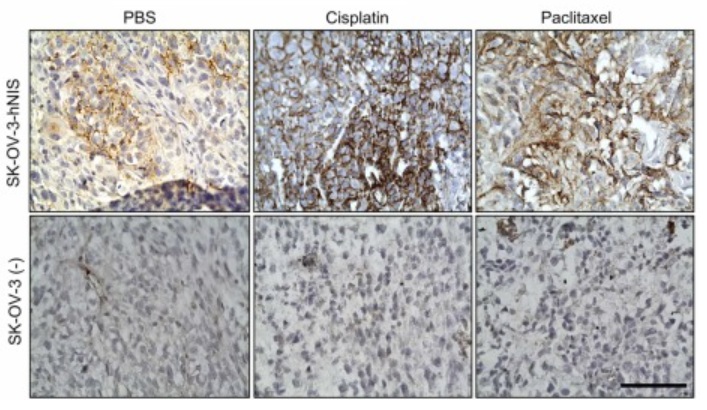
La terapia con radioyodo podría abrir una nueva vía para tratar el cáncer de ovario
Una investigación liderada desde el Instituto de Salud Carlos III (ISCIII) aporta nuevas evidencias científicas de carácter preclínico de que la terapia con radioyodo (I-131), que se utiliza de forma habitual en algunos tumores de tiroides, podría ser una alternativa terapéutica prometedora en cáncer de ovario gracias al uso de una nueva diana, la proteína NIS. El estudio está coordinado por el doctor Antonio de la Vieja Escolar, desde la Unidad de Tumores Endocrinos de la Unidad Funcional de Investigación en Enfermedades Crónicas (UFIEC-ISCIII), y sus resultados se han publicado en la revista Biomedicine & Pharmacotherapy. El trabajo, llevado a cabo en modelos animales, propone aprovechar la presencia en el tumor de la proteína NIS (simportador sodio/yoduro), capaz de introducir y acumular yodo en las células, para dirigir de forma selectiva el efecto del radioyodo sobre las células tumorales. El cáncer de ovario es el tumor ginecológico con mayor mortalidad y, aunque existen distintas opciones terapéuticas, la supervivencia global y las recurrencias siguen no han mejorado en los últimos años de forma significativa en muchos casos. En este contexto, la investigación ahora publicada explora el potencial de una estrategia ‘dirigida’ basada en la citada proteína NIS, que permitiría tanto el tratamiento de la enfermedad como su monitorización mediante técnicas de imagen no invasivas. El equipo de la UFIEC-ISCIII ha analizado muestras de tumores ováricos de pacientes y datos de cohortes disponibles, y ha podido confirmar la presencia de NIS en tumores epiteliales ováricos. Se ha observado, en una proporción relevante de células tumorales, la localización de esta proteína en la membrana plasmática, una condición necesaria para su función de transporte. En modelos preclínicos, también se ha demostrado la capacidad de detectar tumores con expresión funcional de NIS mediante la tecnología de imagen SPECT/CT, utilizando para ello un radioisótopo trazador. La proteína NIS, ‘puerta de entrada’ para tratamiento y diagnóstico Uno de los hallazgos más relevantes es que, en modelos murinos de cáncer de ovario, la administración de una dosis terapéutica del radioyodo I-131 provocó una reducción marcada del volumen tumoral y, en parte de los casos, la desaparición completa del tumor tras el seguimiento. Además, al comparar esta estrategia con fármacos quimioterápicos habituales -como cisplatino y paclitaxel-, el radioyodo mostró mayor eficacia antitumoral y menos efectos secundarios en los animales. Dado que la expresión de NIS no se perdió por completo tras la quimioterapia, podrían explorarse enfoques terapéuticos combinados o secuenciales. De izquierda a derecha: Lidia Mirela, primera firmante del estudio; Antonio de la Vieja, coordinador de la investigación y último firmante (ambos de la Unidad Funcional de Investigación en Enfermedades Crónicas del ISCIII), y Mónica Torres, del Centro Nacional de Sanidad Ambiental y también autora del trabajo. En definitiva, el estudio aporta una prueba de concepto preclínica que respalda la necesidad de avanzar hacia nuevas fases de investigación para evaluar esta aproximación en escenarios más cercanos a la práctica clínica, y determinar qué perfiles tumorales podrían beneficiarse más de este enfoque. En el estudio han participado, como parte de la Unidad de Tumores Endocrinos: Lidia M. Mielu, Lucia Rodal Bravo, Dánae Fajardo Delgado y Rafael Hortiguel. También otras áreas y unidades del Instituto, con apoyo en análisis bioinformático y técnicas experimentales (Pilar Martín Duque de Terapias Avanzadas, Sarai Varona e Isabel Cuesta de la Unidad de Bioinformática, Mónica Torres Ruiz del Centro Nacional de Sanidad Ambiental, y Pilar Pallarés, del Animalario). Además, han colaborado también investigadores de otras instituciones, como el Hospital Universitario de Móstoles, el Instituto de Investigaciones Biomédicas Sols-Morreale (CSIC-UAM), y la Universidad Rey Juan Carlos (URJC). • Referencia del artículo: Mielu LM, Rodal-Bravo L, Diego-Hernández C, et al. Targeted radioiodine therapy of ovarian cancer via the sodium/iodide symporter (NIS). Biomedicine & Pharmacotherapy. Volume 193, 2025, 118873, ISSN 0753-3322. https://doi.org/10.1016/j.biopha.2025.118873. Día Mundial contra el Cáncer: impulso del ISCIII a la I+D+I en oncología El ISCIII lleva a cabo investigaciones específicamente dirigidas al cáncer desde varios de sus centros propios, como el Centro Nacional de Epidemiología (CNE), la citada Unidad de Investigación en Enfermedades Crónicas (UFIEC) y el Instituto de Investigación de Enfermedades Raras (IIER). Además, impulsa investigaciones directamente dirigidas a este ámbito a través de organismos adscritos, como la Fundación Centro Nacional de Investigaciones Oncológicas (CNIO) y el Centro de Investigación Biomédica en Red (CIBER-ISCIII), que dispone de un Área específica de trabajo en cáncer (CIBERONC). Desde el año 2018, el ISCIII ha destinado 464,97 millones de euros a la investigación en cáncer y financiado 1.086 proyectos de investigación a través de convocatorias y programas en el marco de la Acción Estratégica en Salud, la principal herramienta de financiación biomédica y sanitaria en España, y el impulso del Proyecto Estratégico para la Recuperación y Transformación Económica (PERTE) de Salud de Vanguardia.
Saber más
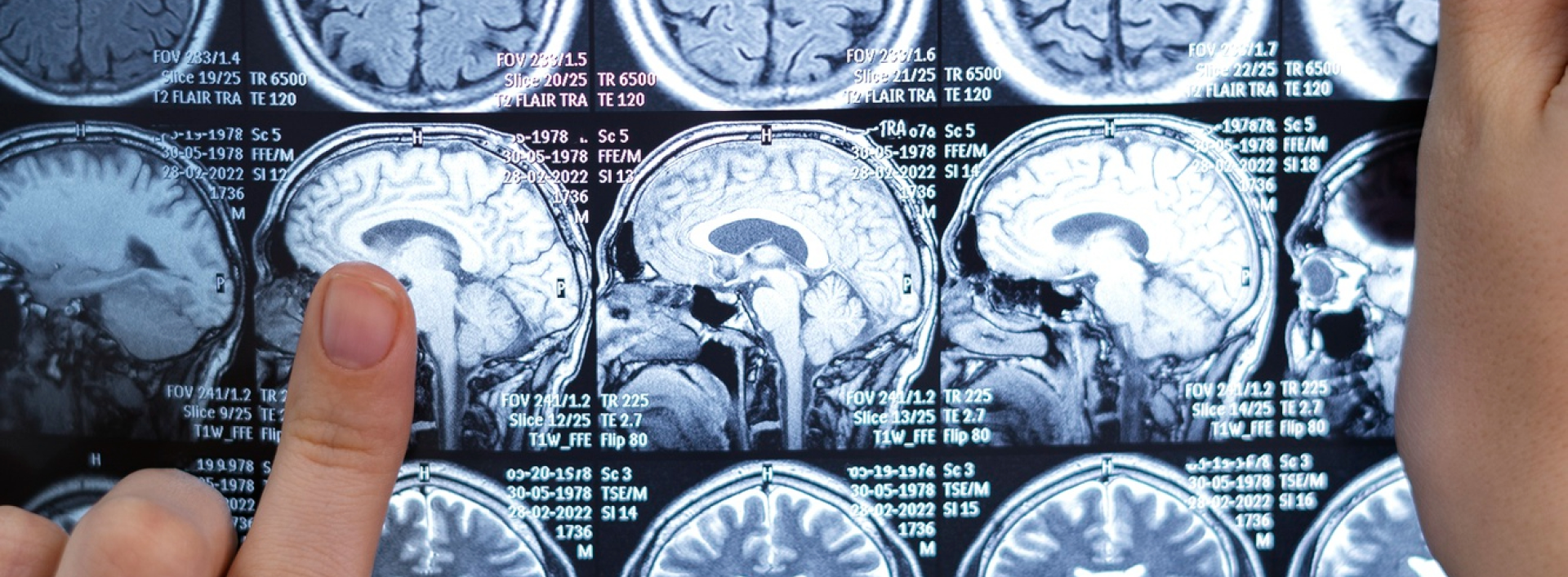
Identificada una posible nueva diana para investigar tratamientos contra el Alzheimer
Un equipo de investigadores del Instituto de Salud Carlos III (ISCIII) ha identificado una proteína que ayuda a regular la formación de placas amiloides en el cerebro, uno de los principales rasgos biológicos de la enfermedad de Alzheimer. El descubrimiento, publicado en la revista Alzheimer’s & Dementia, podría abrir nuevas vías para el desarrollo de futuros tratamientos para esta enfermedad neurodegenerativa. La enfermedad de Alzheimer se caracteriza por la acumulación de proteínas β-amiloides tóxicas, que se agrupan y forman placas que dañan las células cerebrales. Aunque estas proteínas amiloides se han estudiado durante muchos años, la comunidad científica está cada vez más interesada en otras proteínas que interactúan con ellas y que también influyen en la formación de estas placas. En el estudio ahora publicado, los investigadores utilizaron técnicas avanzadas de proteómica para identificar las proteínas que se unen directamente a dos formas de β-amiloide, conocidas como péptidos Aβ40 y Aβ42. Mediante el análisis del tejido cerebral de personas con enfermedad de Alzheimer y de individuos sin demencia, el equipo ha creado un mapa detallado de las proteínas asociadas a las placas amiloides. El trabajo coordinado por Rodrigo Barderas y Ana Montero, de la Unidad Funcional de Investigación en Enfermedades Crónicas (UFIEC) del ISCIII, cuenta con la colaboración de la Unidad de Regeneración Neural de la UFIEC y la Unidad de Microscopía Óptica, la Unidad de Microscopia electrónica y la Unidad de Proteómica de UCCTs del ISCIII, además de la colaboración con investigadores clínicos del Hospital Clínico San Carlos y la Fundación Jiménez Díaz, la Fundación CIEN y la Unidad de Genómica y Proteómica del CIB-CSIC. Según explican los doctores Barderas y Montero, entre las proteínas identificadas hay una que destaca por encima de las demás: PRKCG, una proteína que se encuentra principalmente en las neuronas. El equipo del ISCIII ha demostrado que la alteración de los niveles de PRKCG puede influir en la forma en que las proteínas amiloides se ensamblan en forma de fibrillas, un paso clave en la formación de las citadas placas amiloides precursoras del Alzheimer. Los autores señalan que la proteína PRKCG es potencialmente susceptible de ser una diana para desarrollar posibles fármacos, lo que pondría de relieve una estrategia terapéutica que va más allá de la eliminación de la beta amiloide del cerebro, y que se centraría en la regulación de las proteínas asociadas a la formación de placas. • Referencia del artículo: Montero-Calle A, Coronel R, Manosalva J, Megías D, de Los Ríos V, Rábano A, Peláez-García A, Martínez-Useros J, Fernández-Aceñero MJ, Liste I, Barderas R. Comprehensive profiling of Aβ40 and Aβ42 fibril-interacting proteins reveals PRKCG as a drug-targetable regulator of amyloidogenesis in Alzheimer's disease. Alzheimers Dement. 2026 Jan;22(1):e71090. doi: 10.1002/alz.71090. PMID: 41572619; PMCID: PMC12828073. De izquierda a derecha, Alberto Peláez, Isabel Liste, Rodrigo Barderas, Ana Montero, Juliana Manosalva y Diego Megías, autores del trabajo.
Saber másEmpleo
UFIECPY 110-24-M2 (IND)
Inicio de plazo: 19/05/2026
Fin de plazo: 01/06/2026
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)
SPY 248-22-2PREDOCTORALES
Inicio de plazo: 20/02/2026
Fin de plazo: 05/03/2026
Clase de personal: Laboral
Procedimiento / Modalidad: Predoctoral
IERPY 122/25-BIS-M3-1 INDEFINIDO; INTPY 362/22- M3-4 y 5 INDEFINIDO
Inicio de plazo: 03/12/2025
Fin de plazo: 17/12/2025
Clase de personal: Laboral
Procedimiento / Modalidad: Indefinido (Art. 23 bis LCTI)
ver todas las ofertas